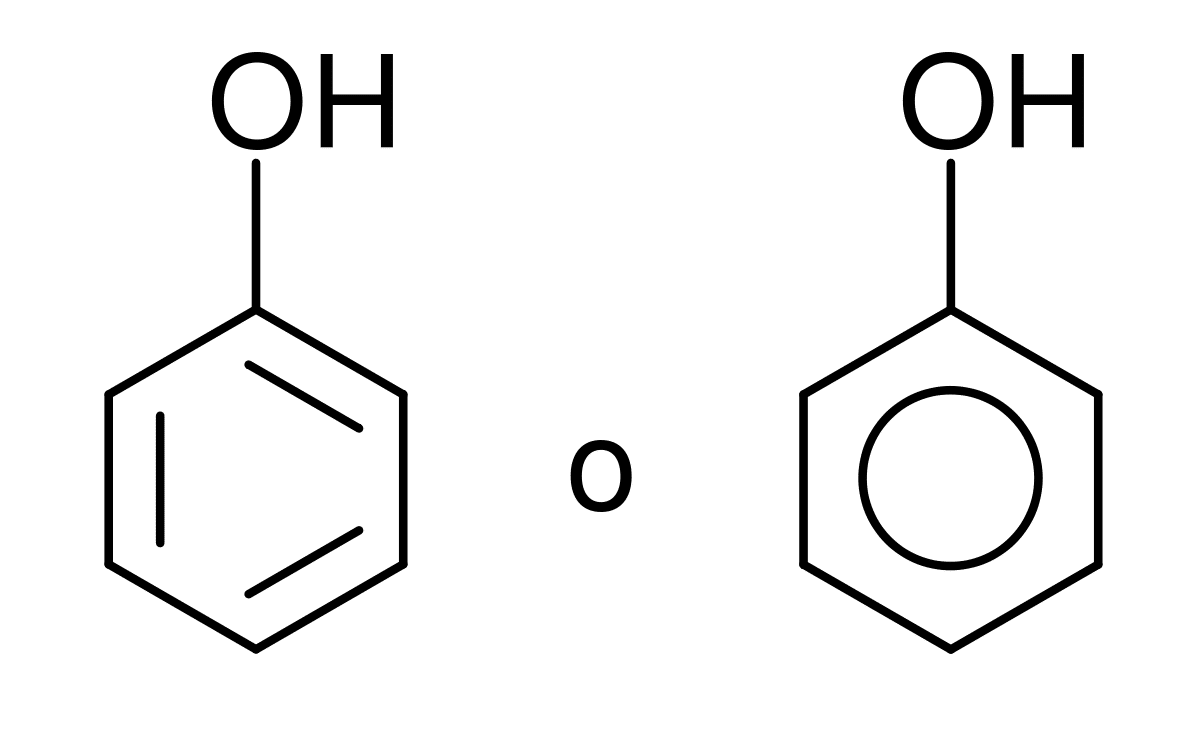
Grupa hidroksil Ona se sastoji od atoma kiseonika i atoma vodonika i nalikuje molekuli vode. Može se naći u raznim hemijskim oblicima, poput grupe, jona ili radikala. Za sve one ljude koji proučavaju organsku hemiju, poznavanje reakcija i važnosti ove grupe atoma je ključno. Sposoban je stvoriti esencijalne veze sa atomom ugljenika, iako to može učiniti i sa sumporom i fosforom.
U ovom članku ćemo vam reći o karakteristikama hidroksilne grupe i značaju koje ona ima u organskoj kemiji.
Glavne karakteristike
Kada analiziramo hidroksilnu skupinu sa stanovišta anorganske hemije, vidimo da ona više učestvuje kao jon. Drugim riječima, vrsta čipke koja postoji između nje i metala nije kovalentna, već jonska. Zbog toga je hidroksilna grupa postala važan element koji pomaže u definiranju svojstava i transformacija mnogih spojeva.
Hidroksilna grupa je vezana za radikal koji je definiran cslovom R ako je alkil ili slovom Ar ako je aromatičan. O znanosti najviše znam šta doprinosi hidroksilnoj grupi molekuli u kojoj se veže. Najbolji odgovor nalazimo u proučavanju njegovih protona. A je li to što se protoni mogu hvatati jakim bazama da bi stvorili soli. Ovo takođe može komunicirati s drugim okolnim skupinama koje su međusobno povezane vodoničnim vezama. Pored toga, najvažnija stvar kod hidroksilne grupe je da, ma gdje se ona nalazila, može predstavljati potencijalno područje za stvaranje vode.
Struktura hidroksilne grupe

Hidroksilna grupa postala je prilično zanimljiv molekul sa stanovišta organske hemije. Molekul vode je uglastog oblika i izgleda poput bumeranga. Ako presiječemo jedan njegov kraj, što znači isto kao uklanjanje protona, mogu se dogoditi razne situacije. Molekul vode je transformiran u hidroksilni radikal ili hidroksilni jon. Međutim, obje imaju molekularno linearnu geometriju i nisu elektroničke.
Sve ove veze nastaju zbog činjenice da su orijentirane na dva atoma kako bi mogle ostati poravnate cijelo vrijeme. Isti slučaj nije ni sa hibridnim orbitalama. Ključ hidroksilne grupe koji omogućava da se različite molekule međusobno miješaju trebaju vodikove veze. Te vodonične veze same po sebi nisu jake, ali kako se broj izvora i broj hidroksilnih grupa u strukturi povećavaju, efekti se množe. Ovo povećanje broja vodoničnih veza odražava se i na fizičkim svojstvima spoja.
Vodikove veze zahtijevaju da atomi budu jedan nasuprot drugom. Postoje neki atomi kiseonika jedne hidroksilne grupe koji moraju biti raspoređeni na takav način da može stvoriti ravnu liniju sa vodikom druge grupe. Ovo je nešto složenije, ali se često događa. Na taj način nastaju sasvim specifični prostorni aranžmani kao što su šta se događa unutar strukture molekula DNK. To se događa između azotnih baza koje čine DNK.
Broj hidroksilnih grupa možemo nazvati strukturom koja je direktno proporcionalna afinitetu vode za molekulu. Daćemo primjer da bismo ga bolje razumjeli. Iako šećer ima hidrofobnu strukturu ugljika, budući da ima veliki broj hidroksilnih grupa, čini ga vrlo topljivim u vodi.
Joni i njihove funkcije
Hidroksilna grupa i jon su vrlo slični, ali imaju različita hemijska svojstva. Hidroksilni jon je izuzetno jaka baza i djeluje hvatanjem protona. Ako ga prisilimo, može se pretvoriti u vodu. A ovo je nepotpuni molekul vode koji je negativno nabijen i kojem je potreban proton da bi ga dovršio. S druge strane, budući da je hidroksilna grupa nema potrebu za hvatanjem protona da bi ga dovršio ponaša se kao izuzetno slaba baza. Sposoban je donirati protone, iako to čini samo protiv baza koje su vrlo jake.
Pozitivne jezgre su atomi u molekuli koji pate od elektroničkog nedostatka kao rezultat svog elektronegativnog okruženja.
Hidroksilna grupa i meteorologija

Znamo da djeluje kao vrsta deterdženta u zraku koji razgrađuje druge plinove. Znamo da je hidroksilna grupa glavna kontrola koncentracije metana. Plin metan je staklenički plin koji je koncentracijom nadmašen samo za ugljen-dioksid u njegovom doprinosu globalnom zagrijavanju. Iako se plin metan nalazi u manjoj mjeri u atmosferi, on može zadržati veću količinu toplote od ugljičnog dioksida.
Novo je istraživanje koje je vodio NASA-in postdoktorand pokazalo da se hidroksilni radikali sami recikliraju i sposobni su održavati konstantnu atmosfersku koncentraciju. Ova koncentracija se održava tokom vremena čak i ako se emisije metana povećavaju. Stoga je razumijevanje uloge hidroksila neophodno za razumijevanje korisnog vijeka metana i atmosfere.
Naučnici su istakli da bi povećane koncentracije i emisije metana mogle dovesti do iscrpljivanja količine hidroksilnih radikala na globalnom nivou. Na taj bi se način produžio vijek trajanja metana, što bi problem dodao globalnom zagrijavanju. Ako bismo produžili životni vijek metana, ne bismo imali čime očistiti atmosferu. Primijećeni su primarni izvori hidroksila i metana i kako oni reagiraju. Recikliranje ove skupine događa se nakon što se metan razgradi, a zatim reformiše u prisustvu drugih plinova. Koncentracije hidroksila s vremenom su prilično stabilne. Ne bi trebali nužno nestati kad reagira s metanom.
Nadam se da ćete s ovim informacijama saznati više o hidroksilnoj grupi i svim njenim važnostima.