
След запознанството Атомният модел на Томсън, който счита, че електроните са в положително заредена среда, по-усъвършенстван модел, известен като Ръдърфордски атомен модел. Ученият, отговорен за този нов напредък в науката, беше Ърнест Ръдърфорд. Той е роден на 20 август 1871 г. и умира на 19 октомври 1937 г. По време на живота си той има голям принос в химията и света на науката като цяло.
Затова ще посветим тази статия, за да ви разкажем всичко, което трябва да знаете за атомния модел на Ръдърфорд.
Експеримент със златни листа
Старият модел на thomson казва, че електроните са в положително заредена среда. През 1909 г. Ърнест Ръдърфорд, придружен от двама асистенти на име Гейгер и Марсден, направи проучване, известно като експеримент със златни листа, където те могат да проверят Известният „пудинг от стафиди“ на Томсън беше погрешен. И е, че този нов експеримент успя да покаже, че атомът има структура със силен положителен заряд. Този експеримент или може да помогне за възстановяване на някои заключения, които в крайна сметка са представени като атомния модел на Ръдърфорд през 1911 г.
Експериментът, известен като Лист от злато, не е уникален, но е проведен между 1909 и 1913 г. За това те са използвали физическите лаборатории на Университета в Манчестър. Тези експерименти са били от голямо значение, тъй като от техните резултати могат да се направят нови заключения, които са довели до революционен атомен модел.
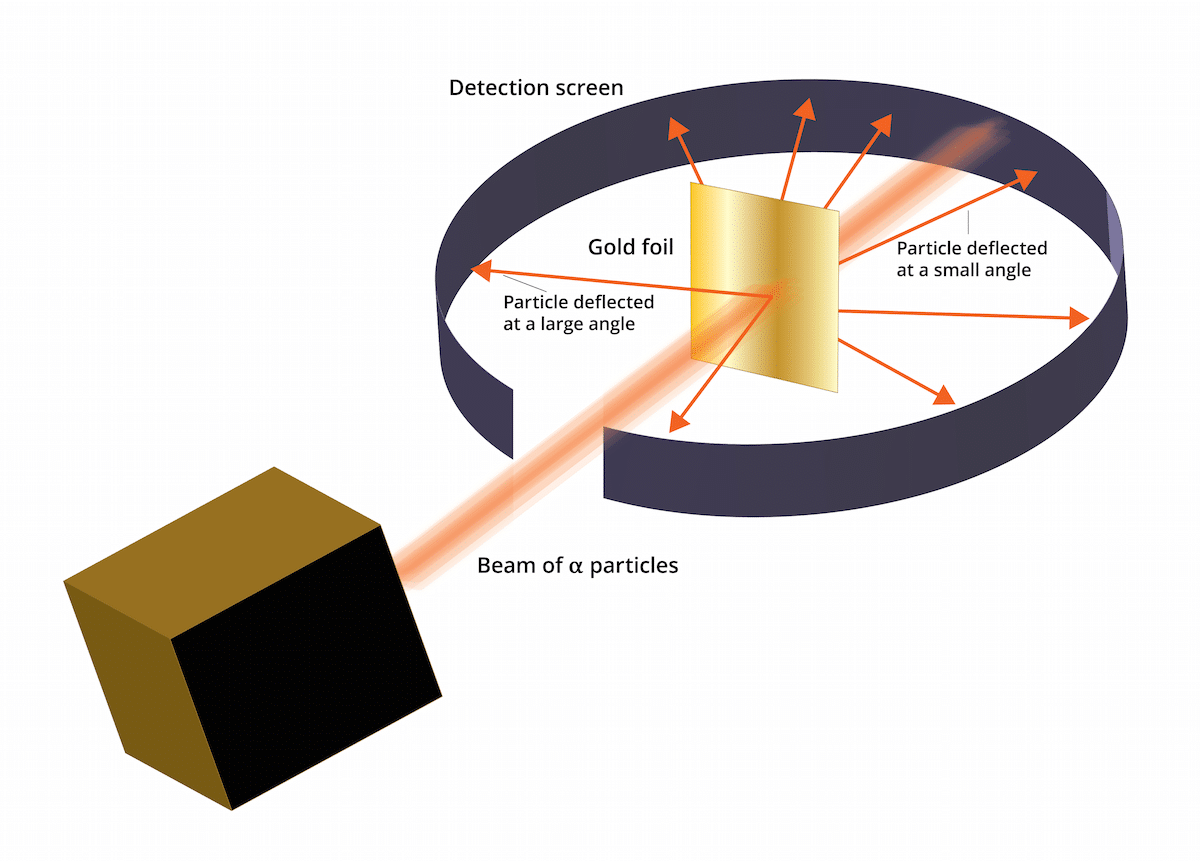
Този експеримент се състоеше от следното: тънък лист злато с дебелина само 100 nm трябваше да бъде бомбардиран с голямо количество алфа частици. Тези алфа частици бяха и йони. Тоест атоми, които нямат електрони, така че те са имали само протони и неутрони. Като има неутрони и протони, общият заряд на атома е положителен. Този експеримент основно имаше за цел да потвърди дали моделът на Томсън е правилен. Ако този модел беше прав, алфа частиците трябваше да преминат през златните атоми по права линия.
За да се изследва деформацията, причинена от алфа частици, около финото златно фолио трябваше да се постави флуоресцентен филтър от цинков сулфид. Резултатът от този експеримент е, че е забелязано, че някои частици са били в състояние да преминат през златните атоми на листа по права линия. Някои от тези алфа частици обаче се отклоняват в произволни посоки.
Заключения от експеримента със златни листа

Предвид този факт не беше възможно да се потвърди това, което се счита за предишните атомни модели. И то е, че тези атомни модели посочват, че положителният заряд е разпределен равномерно в атомите и това ще улесни преминаването му, тъй като зарядът му няма да бъде толкова силен в определена точка.
Резултатите от този експеримент със златни листа бяха напълно неочаквани. Това накара Ръдърфорд да мисли, че атомът има център със силен положителен заряд, който създава алфа частица опитайте се да го предадете отхвърлен от централната структура. За да се установи по-надежден източник, частиците се разглеждат в количества от отразените и тези, които не са. Благодарение на тази селекция от частици беше възможно да се определи размерът на ядрото в сравнение с орбитата на електроните, които са около него. Може също да се заключи, че по-голямата част от пространството на атома е празно.
Виждаше се, че някои алфа частици се отклоняват от златното фолио. Някои от тях се отклоняваха само под много малки ъгли. Това помогна да се заключи, че положителният заряд върху атом не е равномерно разпределен. Тоест положителният заряд се намира върху атом концентрирано в много малък обем пространство.
Много малко алфа частици се отклониха назад. Това отклонение показва, както следва, че споменатите частици биха могли да се възстановят. Благодарение на всички тези нови съображения, атомният модел на Ръдърфорд може да бъде създаден с нови идеи.
Ръдърфордски атомен модел

Ще проучим какви са принципите на атомния модел на Ръдърфорд:
- Частици, които имат положителен заряд вътре в атома те са подредени в много малък обем, ако го сравним с общия обем на споменатия атом.
- Почти цялата маса, която има атомът, е в споменатия малък обем. Тази вътрешна маса се нарича ядро.
- Електрони, които имат отрицателни заряди се намират въртящи се около ядрото.
- Електроните се въртят с висока скорост, когато са около ядрото и го правят по кръгови пътеки. Тези траектории бяха наречени орбити. По-късно ще го направя те са известни като орбитали.
- Както електроните, които са били отрицателно заредени, така и ядрото на самия положително зареден атом, винаги се държат заедно благодарение на електростатичната сила на привличане.
Приемане и ограничения на атомния модел на Ръдърфорд
Както се очакваше, този нов модел предвиждаше изцяло нова панорама на атома в научния свят. Благодарение на този атомен модел много по-късни учени биха могли да изучат и определят броя на електроните, които има всеки елемент в периодичната таблица. Освен това могат да се направят нови открития, които да помогнат да се обясни функционирането на атома по най-простия начин.
Този модел обаче има и някои ограничения и грешки. Въпреки че това беше пробив в света на физиката, те не бяха нито перфектен, нито пълен модел. И това ли е на според законите на Нютон и важен аспект от законите на Максуел, този модел не може да обясни някои неща:
- Той не можеше да обясни как отрицателните заряди могат да се задържат в ядрото. Според електронната пищяла положителните заряди трябва да се отблъскват.
- Друго противоречие беше към основните закони на електродинамиката. Ако се смята, че електроните с положителен заряд се въртят около ядрото, те трябва да излъчват електромагнитно излъчване. При излъчването на това излъчване се изразходва енергия, за да се срутят електроните в ядрото. Следователно набразденият атомен модел не може да обясни стабилността на атома.
Надявам се, че с тази информация можете да научите повече за атомния модел на Ръдърфорд.