
عندما نتحدث عن الديناميكا الحرارية ، فإن الكون. إنتروبيا النظام هي نوع من قياس الطاقة غير متوفر في نظام ديناميكي حراري أو نظام مغلق والذي يُنظر إليه أيضًا على أنه مقياس لاضطراب النظام. إنها خاصية لحالة النظام تختلف بشكل مباشر مع أي تغيير ، طالما أنها قابلة للانعكاس في حرارة النظام أو عكسها مع درجة حرارة النظام.
سنخبرك في هذه المقالة بكل ما تحتاج لمعرفته حول الانتروبيا وسنقدم لك بعض الأمثلة في الحياة اليومية.
تعريف الانتروبيا

نحن نعلم أنه مقياس الطاقة غير المتاح داخل نظام حراري مغلق. إحدى طرق استخدام الانتروبيا هي قياس اضطراب النظام. ذلك بالقول، الفوضى داخل النظام بسبب الانتروبيا. عادة ، مع ارتفاع درجة الحرارة أو انخفاضها ، يحدث ذلك عندما تكون هناك تغييرات كبيرة في الجزيئات والذرات التي تشكل النظام.
إذا قمنا بتعريف الانتروبيا بمصطلحات أبسط ، فيمكننا القول إنها تدهور للمادة والطاقة في الكون إلى حالة نهائية من الانتظام الخامل.
الملامح الرئيسية
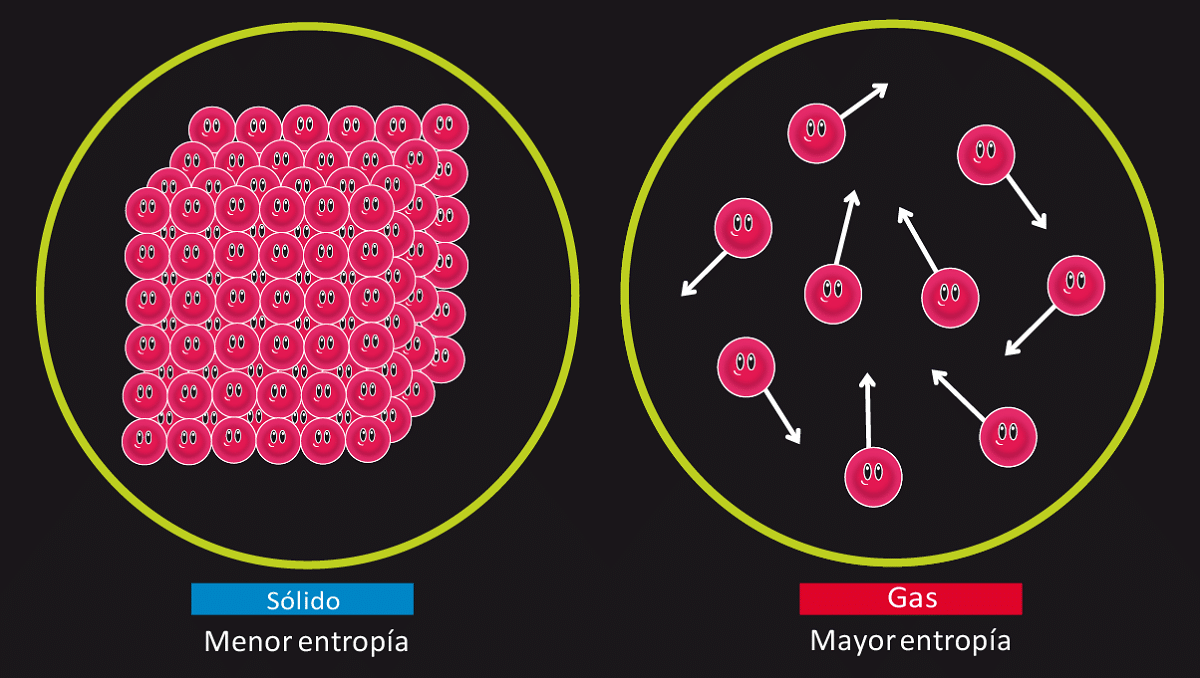
سنرى ما هي الخصائص الرئيسية التي تشمل الإنتروبيا. لها ثلاث خصائص رئيسية. أحدها هو أن إنتروبيا النظام تزداد عندما يتم توفير الحرارة في النظام بغض النظر عما إذا كانت درجة الحرارة تزداد أيضًا نتيجة لذلك. وهذا يعني أنه في أي نظام نقدم فيه الحرارة ، تزداد إنتروبيا النظام.
عندما ندخل الحرارة إلى نظام بيئي ، سواء تغيرت درجة الحرارة أم لا ، فإن الانتروبيا تنخفض عندما يتم رفض هذه الحرارة. في في جميع العمليات التي تكون ثابتة الحرارة ، تظل قيمة الانتروبيا ثابتة بمرور الوقت. يجب أن يتم قياس الانتروبيا بحذر شديد. وهي أنه عند قياسها ، يجب اتخاذ قرارات تعسفية ويمكن تجنب بعضها. على سبيل المثال ، وحدة التقسيم ، مع أخذ ما يسمى معدل الانتروبيا ، لكن بعض القيود الأخرى لا يمكن التغلب عليها.
دعنا نضع مثالاً لتوضيح هذا بشكل أفضل. إذا كان علينا أن نختار كيفية وصف أحداث معينة تحدث لأن الانتروبيا ليست ثابتة ، فيمكننا وصف نفس الكائن بنفس الطريقة. هذا قيد أكبر من القيد الشائع ومن المسلم به عمومًا أنه من أجل قياس الإنتروبيا ، يجب معرفة مجال المشكلة المراد معالجتها.
ومع ذلك ، يمكننا تعريف الإنتروبيا على أنها وظيفة بسيطة للغاية. إنه يحتوي على لوغاريتم واحد فقط وعدد الأشياء التي لها خصائص معينة تهم.
خصائص الانتروبيا

سنبدأ في وصف أهم خصائص الانتروبيا في تجربتنا اليومية. يمكن تقديمه كشيء ليس له وزن و يمكن أن تتدفق في كل شيء في عالمنا. إنها خاصية لها علاقة بكمية المادة في الجسم والتي تشير إلى منطقة من الفضاء ويمكن التعامل معها بشكل أساسي على أنها مادة. في هذا الطريق، يمكن توزيع الإنتروبيا على مساحة من المادة ، متراكمة بشكل عكسي أو مباشر. يمكن أيضًا استخراجها أو فك ضغطها أو نقلها إلى كائن آخر. بهذه الطريقة ، يمكننا ربطها بطاقتنا.
نحن نعلم أن الانتروبيا تغير حالة الجسم بشكل كبير. عندما تكون المادة منخفضة الكمية ، يُنظر إليها على أنها باردة. إذا كانت الأسطورة المادية تحتوي على المزيد والمزيد من كمية الانتروبيا ، فيمكن اعتبارها أكثر طلبًا. لهذا السبب نعلم أنه يلعب دورًا أساسيًا في جميع الجوانب الحرارية ويمكن اعتباره سببًا لهذه التأثيرات. بدون هذا القياس لا توجد درجة حرارة أو حرارة. يميل عادةً إلى الانتشار في جميع أنحاء الجسم المتجانس ويتم تدميره تلقائيًا بسرعة أو أقل بشكل موحد في جميع أنحاء الحجم.
في هذه العملية ، يمكننا أن نرى أن الانتروبيا تتدفق من الجسم الأكثر حرارة إلى الجسم الأكثر برودة. هناك مواد موصلة جيدة مثل الفضة والنحاس والألماس والألمنيوم وغيرها من المواد السيئة التي تجعلها تتدفق بشكل أبطأ مثل الخشب أو البلاستيك أو الهواء. بينما نستخدم في حياتنا اليومية موصلات جيدة لنقلها ، فإننا نستخدم موصلات سيئة كعوازل.
يتم إنتاج كمية كبيرة من الانتروبيا في ملف التسخين لمحطة الطاقة. تحدث أيضًا في لهب موقد الزيت وعلى أسطح الاحتكاك لنظام الفرامل القرصية. مكان آخر حيث يتم تكوين كمية كبيرة هو في عضلات رياضي في حالة حركة مستمرة. نفس الشيء صحيح في الدماغ. عندما نفكر ، يتم إنتاج الكثير من الانتروبيا.
درجة الحرارة والطبيعة
نحن نعلم عمليًا أن الإنتاج يحدث في كل حالة في الطبيعة. في أي موقف يوجد فيه تغيير ، هناك إنتروبيا متضمنة. أكثر ما يثير الدهشة هو أنه يحدث عمليا في جميع العمليات التي تحدث في الحياة ، سواء بكميات صغيرة أو كبيرة. لا توجد حاليًا آلية معروفة يمكن بواسطتها ، بمجرد إنتاج كمية الانتروبيا ، لا يمكن تدميرها. يمكن أن يزيد إجمالي الكمية الحالية فقط ولا ينقص أبدًا.
أي عملية تولد الإنتروبيا لا يمكنها إعادة هذه الطاقة لأنها نظام لا رجوع فيه. هذا لا يعني أن الجسم يمكن أن يعود إلى حالته الأولية ، فقط أن هذه الكمية من الحرارة تغادر جسمك. الادعاء بأنها تزيد ولا تنقص هذا هو ما ورد في القانون الثاني للديناميكا الحرارية. إذا لم يكن هناك مكان لإيداع الإنتروبيا ، فلا يمكن للجسم أن يعود إلى حالته الأولية.
كما ترى ، من الصعب وصفها ولكنها مفيدة جدًا على أساس يومي. آمل أن تتمكن من خلال هذه المعلومات من معرفة المزيد حول هذا الموضوع.